1.2.1. Новый энергетический параметр стабильности кристаллического вещества — энергия сцепления атомных остовов и связующих электронов
До недавнего времени были известны два энергетических подхода к кристаллическому веществу: 1) основанный на концепции энергии кристаллической ионной решетки (энергии разрыва кристалла на свободные составляющие ионы) и 2) основанный на концепции энергии атомизации (энергии разрыва кристалла на свободные нейтральные составляющие атомы).
Следует признать, что по сравнению с ведущим вторым подходом первый энергетический подход имеет менее универсальный характер и соответственно ограниченные возможности в смысле предсказания физических свойств разнообразных кристаллических соединений и, в частности, металлов. Поэтому некоторые современные ученые не только предают забвению первый энергетический подход, но и фактически предлагают от него отказаться, как от устаревшего и неудовлетворительного. Хотя мы и не вполне разделяем эту точку зрения, однако в указанной ситуации разработка (предложение) еще одного принципиально нового конкурентноспособного энергетического подхода к кристаллам (и оценке их разнообразных физических свойств) представляется вполне оправданной, актуальной и целесообразной.
Как оказалось, теоретически возможен также третий энергетический подход к кристаллам, основанный на остовно-электронном моделировании их строения (Зуев, 1990). Напомним, что остовно-электронная концепция рассматривает кристаллическое соединение, независимо от типа химической связи, состоящим из положительно заряженных атомных остовов
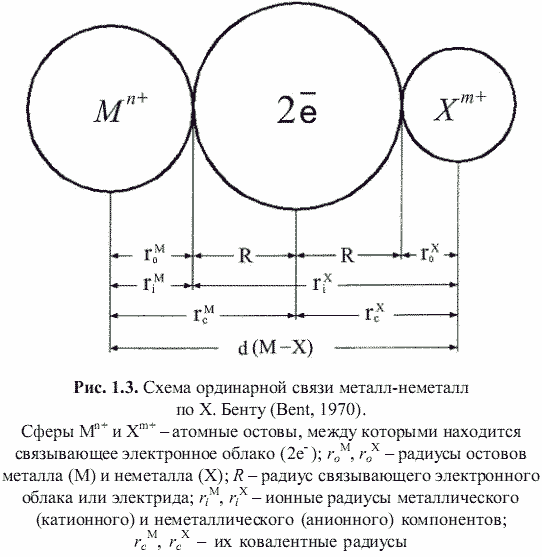
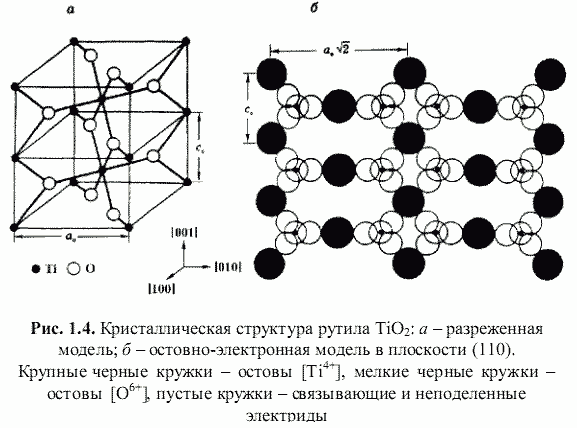
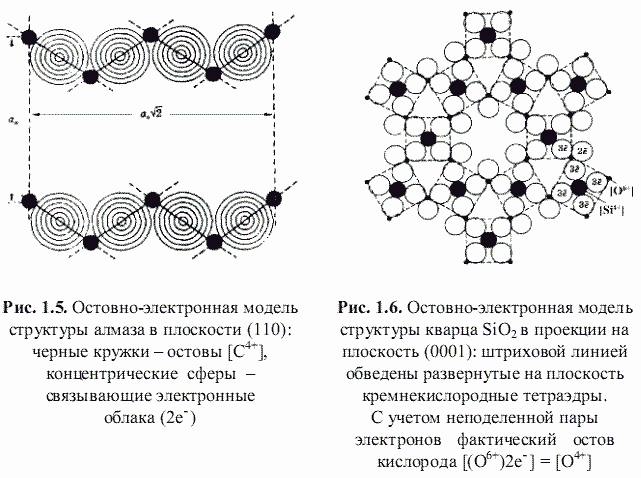
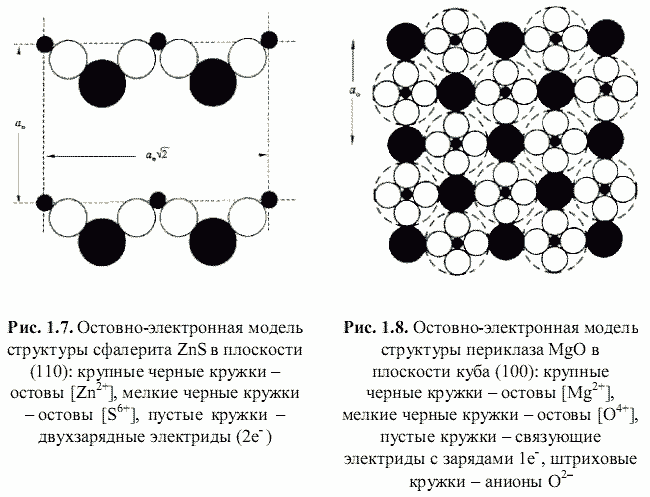
[1] (как металла, так и неметалла) и связывающих или поделенных (а также несвязывающих или неподеленных) валентных электронов. Принимая для тех и других, согласно (Bent, 1970; Зуев, 1990), сферическую форму (рис. 1.3), были построены соответствующие остовно-электронные модели кристаллических структур минералов, примеры которых приведены на рис. 1.4-1.8. Связывающие электронные облака можно именовать электридами, а соответствующие модели - остовно-электридными. Таким путем удается описать (хотя и с известной долей упрощения) строение соединений всех без исключения классов - будь то металлы, ковалентные или ионные кристаллы.
[2]
Естественно предположить, что основу сцепления положительных остовов и отрицательных электридов в моделях типа изображенных на рис. 1.4-1.8 будет составлять электростатическое взаимодействие, энергию которого можно рассчитать в рамках концепции кристаллической ионной решетки, в которой атомные остовы являются катионами, а электриды - анионами. И, как нам представляется, наряду с энергией классической ионной решетки и энергией атомизации (используемых в первом и втором энергетических подходах), энергия остовно-электронного взаимодействия кристаллов в рамках третьего энергетического подхода может служить объективной мерой их стабильности и использоваться для оценки их свойств подобно тому, как это показано в работах (Зуев, Мочалов, Щербатов, 1998; Зуев, Аксенова, Мочалов и др., 1999). Схематически различие трех указанных энергетических подходов лучше всего продемонстрировать на конкретном примере обладающего тетраэдрической координацией атомов кристалла ZnS (сфалерита):
- ZnS → Zn2+ + S2- + U;
- ZnS → Zn0 + S0 + Eа;
- ZnS → Zn2+ + S6+ + 8e- + W,
где выражаемые в кДж/моль или МДж/моль соответственно:
U - энергия кристаллической решетки,
Еа - энергия атомизации (энергия сцепления атомов),
W - энергия сцепления двух остовов (Zn
2+, S
6+) и четырех двухзарядных электридов (4x2e
-).
Соответствующая остовно-электронная модель для сфалерита, согласно рис. 1.7, -|[Zn
2+](2e
-)
4[S
6+]| т. е. на формульную единицу сфалерита приходится шесть заряженных частиц (два остова и четыре электрида). Остовно-электронная модель периклаза (рис. 1.8) - |[Mg
2+](1e
-)
6[O
4+]| - содержит два остова и шесть электридов (восемь частиц). Важно подчеркнуть, что если координационное окружение остовов электридами соответствует координационным числам (
КЧ) атомов соединения, то для всех электридов имеет место линейная координация остовами (
КЧ = 2).
В результате уточнения и дополнения классической формулы ионной кристаллической решетки (Урусов, 1975, с. 23; Харрисон, 1983, с. 22), нами была выведена следующая формула энергии сцепления остовов и электридов для общего случая кристаллического соединения
[3]:
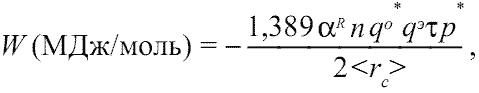 (1.9)
(1.9)
где: 1,389 - константа для выражения энергии сцепления остовов и электридов в МДж/моль
[4]; α
R - приведенная (связевая) константа Маделунга;
n - суммарное число остовов и электридов, приходящихся на формульную единицу соединения;
qo* - суммарный эффективный заряд ядра, действующий на валентные (сверх остовные) электроны атома;
qэ - заряд электрида; τ - коэффициент отталкивания, равный 0,1¸0,7;
p* - коэффициент, характеризующий ковалентность связей, равный (1-
fi2)
1/2, где
fi - ионность соединения
[5]; 2<
rc>, (Å) - удвоенное среднее межатомное расстояние остов-электрид, равное удвоенным усредненным величинам ковалентных радиусов образующих кристалл атомов. Напомним, что в остовно-электронной модели ковалентный радиус атома равен сумме соответствующих ионных радиусов остова и электрида. Таким образом, для соединений МxXy, согласно схеме на рис. 1.3, можно записать: 2<
rcM,X> = 2(
rcM +
rcX)/2 =
=
rcM +
rcX =
d(M-X), где
d -межатомное расстояние металл - неметалл в структуре. Следовательно, в знаменателе формулы (1.9) вместо члена 2<
rc> можно поместить параметр
d, Å среднего межатомного расстояния металл - неметалл соответствующего соединения:
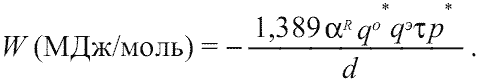 (1.10)
(1.10)
Очевидно, что в случае сложных кристаллических соединений в расчетах по формуле (1.10) необходимо использовать усредненные параметры
qo*,
qэ,
fi,
d.
Как указывалось, вместо номинального заряда остова (например, Na
+, Zn
2+, Al
3+, C
4+, S
6+ и т. д.) в формуле (1.10) используется, согласно (Зуев, 1990; Зуев, Денисов, Мочалов и др., 2000), более адекватно характеризующий силовое поле остова параметр:
qo* = ΣZi*, (1.11)
где
Zi* - эффективные заряды ядра, действующие на валентные электроны и рассчитываемые по формуле (Zhang, 1982):
Z* = n*(Iw/R)1/2, (1.12)
где
n* - эффективное главное квантовое число,
Iw (эВ) - потенциал ионизации атома соответствующей валентности (w),
R - потенциал ионизации атома водорода, равный 13,595 эВ.
Например, расчеты по этим формулам дают для остовов:
[Na
+] -
qo*= 2,89(5,138/13,595)
1/2 = 1,78;
[Zn
2+] -
qo* = 3,45(9,391/13,595)
1/2 + 3,45(17,96/13,595)
1/2 = 6,83;
[C
4+] -
qo* = 1,99(11,264/13,595)
1/2 + 1,99(24,376/13,595)
1/2 +
+1,99(47,86/13,595)
1/2 + 1,99(64,48/13,595)
1/2 = 12,54;
[S
6+] -
qo* = 2,89(10,357/13,595)
1/2 + 2,89(23,4/13,595)
1/2 +
+ 2,89(34,8/13,595)
1/2 + 2,89(47,29/13,595)
1/2 +
+ 2,89(72,5/13,595)
1/2 + 2,89(88/13,595)
1/2 = 30,35 и т. д.
Необходимо объяснить сравнительно малую величину (0,1-0,7) коэффициента отталкивания, который в случае ионных кристаллических решеток гораздо выше (около 0,9). С одной стороны, это связано со значительным ростом положительных зарядов
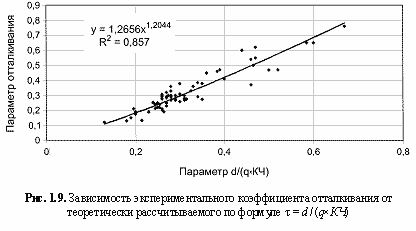
qo* по сравнению с соответствующими номинальными. С другой стороны, остовно-электронные модели кристаллов являются по образному выражению Бента (Bent, 1970) постройками из «ионов внутри ионов», что наглядно показано на примере периклаза на рис. 1.8. Этими обстоятельствами и объясняется столь сильное взаимное отталкивание одноименно заряженных частиц в остовно-электридных моделях. Обычно параметр t находится из данных по сжимаемости кристаллов. Нами для его оценки была выведена (рис. 1.9) следующая эмпирическая формула:
τ = 1,2656[d/(qxКЧ)]1.2, (1.13)
где
d - межатомное расстояние в структуре;
q - заряд электрида;
КЧ - координационное число атомов (для сложных кристаллов все эти параметры являются средними для рассматриваемой структуры величинами).
Следует специально остановиться на оценке константы Маделунга α
R, строгий вывод которой для сложных остовно-электронных моделей структур весьма трудоемок. Поэтому нами принят упрощенный метод ее расчета по формуле Темплтона (Урусов, 1975):
αR = 1,89 - 1/n x Σni/КЧi. (1.14)
Здесь
ni - число частиц (остовов, электридов)
i-сорта с соответствующими координационными числами;
n - общее число остовов и электридов, приходящихся на формульную единицу соединения.
Например, для имеющего в своем составе два остова и четыре электрида сфалерита ZnS расчет по формуле (1.14) приводит к
α
R = 1,89 - (2/4 + 4/2)/6 = 1,473. Для периклаза MgO (с двумя остовами и шестью электридами) получается такая же величина α
R = 1,89 - (2/6 + 6/2)/8 = 1,473. Если (см. рис. 1.6) неподеленную пару электронов включить в остов атома кислорода, то остовно-электронная модель кварца будет |[Si4+](3e-)
4[O4+]
2|, и в этом случае α
R = 1,89 - (1/4 + 2/2 + 4/2)/7 = 1,426.
Остановимся также подробнее на физическом смысле параметра
р* в формуле (1.10). С этой целью рассмотрим ряд изоэлектронных и изоструктурных (типа сфалерита) соединений GeGe, GaAs, ZnSe, CuBr (таблица 1.10). Если обратиться к остовно-электронным схемам отдельных межатомных связей: [Ge
4+](2e
-)[Ge
4+], [Ga
3+](2e
-)[As
5+], [Zn
2+](2e
-)[Se
6+] и [Cu
1+](2e
-)[Br
7+] этих соединений, то они оказываются практически идентичными по всем кристаллохимическим параметрам (средним зарядам остовов, зарядам электридов, межатомным расстояниям и др.), по величинам энергий гипотетических неполярных (λ = 0) ковалентных связей, а также по величинам формульных весов, мольных объемов и плотностей. Тем не менее, в ряду CuBr→ZnSe→GaAs→GeGe имеет место явно ощутимый, закономерный рост термодинамической и механической стабильности соединений (фиксируемый соответствующим увеличением их энергоплотности
Ev и относительной твердости
НМ).
Таблица 1.10
Взаимосвязь термодинамической и механической прочности тетраэдрически координированных кристаллов с параметрами ионности/ковалентности химических связей
| Кристалл |
М,г/моль |
D(M-X)λ=0,кДж/моль |
Ev,кДж/см3 |
НМ, отн.ед. |
fi |
р* |
| GeGe |
145,18 |
187,4 |
27,6 |
6 |
0 |
1 |
| GaAs |
144,64 |
186,5 |
24 |
5 |
0,30 |
0,95 |
| ZnSe |
144,34 |
183,6 |
19,6 |
4 |
0,53 |
0,85 |
| CuBr |
143,45 |
182,4 |
18,2 |
2,5 |
0,73 |
0,68 |
Единственным объяснением этого феномена является различие в ионности (
fi) рассматриваемых соединений, что и предлагается учитывать в формуле (1.10) введением параметра
р*, отражающего ковалентность/полярность межатомных связей или, другими словами, асимметрию распределения электридов в межостовном пространстве. Естественно допустить, что ковалентные неполярные связи типа Ge-Ge (с симметричным распределением межостовных электридов) будут прочнее полярных связей типа Cu-Br (с асимметричным распределением межостовных электридов). Соответственным образом энергия сцепления электрида с остовами в последнем случае будет меньше. Расчеты показали, что учет рассматриваемого фактора обеспечивается введением в формулу (1.10) коэффициента
р* = (1-
fi2)
1/2, ранее использованного В. С. Урусовым при оценке вклада ковалентной составляющей в энергию атомизации полярных кристаллов (Урусов, 1975).
Далее, располагая соответствующими данными, рассчитаем в качестве примеров энергии сцепления остовов и электридов для алмаза, сфалерита, периклаза, галита, кварца, металлического железа и форстерита. Принятые в них валентности атомов и соответствующие заряды атомных остовов и связующих электридов энергетически обоснованы в следующем разделе 1.2.2.
В случае алмаза остовно-электронная формула - |[C
4+](2e
-)
4[C
4+]|, подставляя в формулу (1.10) α
R = 1,473,
n = 6,
qo* = 12,54,
qэ = -2,
τ = 0,15,
р* = 1 и
d = 1,54 Å, получаем
W = 29,99 МДж/моль. Расчет выполнен для двухатомной стехиометрии соединения (СС).
Для сфалерита ZnS расчет с использованием α
R = 1,473,
n = 6, <
qo*> = (6,83 + 30,35)/2 = 18,59,
qэ = -2, τ = 0,3,
р* = 0,53 (
fi = 0,85) и
d = 2,35 Å дает
W = 29,85 МДж/моль.
Для периклаза MgO (α
R = 1,473,
n = 8, <
qo*> = (5,21 + 13,94)/2 = 9,575,
qэ = -1, τ = 0,6,
р* = 0,465 (
fi = 0,885),
d = 2,10 Å) получается
W = 20,82 МДж/моль.
Для галита NaCl, остовно-электронная формула которого - |[Na
1+](1e
-)
6[Cl
5+]|, расчет с использованием α
R = 1,473,
n = 8,
<
qo*> = (1,78 + 23,71)/2 = 12,745,
qэ = -1, τ = 0,6,
р* = 0,455 (
fi = 0,89), d = 2,82 Å дает
W = 20,2 МДж/моль.
Для кварца SiO
2 расчет с использованием a
R = 1,430,
n = 7, <
qo*> = (15,205 + 13,94x2)/3 = 14,36,
qэ = -3, τ = 0,157,
р* = 0,8 (
fi = 0,6),
d = 1,61 Å приводит к
W = 46,73 МДж/моль.
Металлическое железо (модификации a-Fe) обладает объемно-центрированной кубической решеткой с
КЧ = 8, остовно-электронная модель, согласно (Зуев, 1997) - |[Fe
4+](1e
-)
8[Fe
4+]|. По формуле (1.14) α
R = 1,89 - (2/8 + 8/2)/10 = 1,465. Используя этот и другие необходимые параметры, по формуле (1.10) находим
W = (1,389x1,465x10x16,6x1x0,16x1)/2,48 = 21,8 МДж/моль. Как и в случае алмаза, эта энергия относится к двухатомной стехиометрии соединения, в расчете на одноатомную стехиометрию (Fe)
W = 10,9 МДж/моль.
Остовно-электронная модель форстерита Mg
2SiO
4 содержит 23 заряженных частицы: 2 остова [Mg2+], 1 остов [Si4+], 4 остова [O4+] и 16 электридов (соответствующих 12 связям Mg-O и 4 связям Si-O в формульной единице соединения). Суммарный заряд остовов равен +24, а средний заряд электрида <
qэ> = -24/16 = -1,5. Средний параметр <
qo*> = (5,21x2 + 15,205 + 13,94x4)/7 = 11,63. По формуле (1.14) α
R = 1,89 - (2/6 + 1/4 + 4/4 + 16/2)/23 = 1,473. Среднее межатомное расстояние <
d> = (2,12x6x2 + 1,64x4)/16 = 2,0 Å, t = 0,3,
fi = 0,7 и
р* = 0,71. По формуле (1.10) получается
W = 87,43 МДж/моль.
В принципе, проконтролировать найденные параметры
W минералов можно по формуле:
W (МДж/моль) = 8,032x0,0965φn = 0,775φn, (1.15)
где 8,032 - коэффициент пропорциональности, увязывающий эту формулу с формулой (1.10); 0,0965 - константа (1 эВ = 0,0965 МДж/моль); φ - работа выхода электрона из кристаллического соединения, эВ;
n - общее число валентных электронов в формульной единице соединения, равное, как это очевидно, суммарному заряду остовов.
Правомерность формулы (1.15) очевидна, поскольку энергия выхода из кристалла всех валентных электронов соответствует нарушению сил их сцепления с атомными остовами и разрушению кристалла вследствие взаимного отталкивания последних.
Однако экспериментальных данных о параметрах φ минералов, как и неорганических кристаллов вообще, очень мало. Поэтому, используя найденные по формуле (1.10) величины
W и подставляя их в формулу (1.15), можно вычислять параметры j практически для любых кристаллических соединений и минералов. Примеры таких оценок j для некоторых кристаллов даны в таблице 1.11, в которой экспериментальные данные взяты из (Поверхностные свойства твердых тел, 1972; Физико-химические свойства окислов, 1978).
Возможны также другие весьма эффективные пути контроля рассчитываемых по формуле (1.10) энергий сцепления остовов и электридов в кристаллах (Зуев, 2005). Если, затратив энергию
W, разделить кристалл на составляющие его остовы и электриды, а затем путем рекомбинации электронов остовами вернуть их в состояние нейтральных свободных атомов с выделением соответствующей энергии, то разность этих двух энергий будет, очевидно, представлять энергию атомизации (энергию сцепления атомов) рассматриваемого соединения:
Eα = W - ΣIn, (1.16)
где Σ
In - суммарный потенциал ионизации составляющих кристалл свободных нейтральных атомов до состояния остовов (или, что то же самое, энергия рекомбинации электронов остовами до состояния нейтральных атомов). Потенциалы ионизации атомов являются справочными величинами (Свойства элементов, 1976), однако обычно они приводятся в эВ, для перевода их в МДж/моль служит соотношение 1 эВ = 96,486 кДж/моль = 0,0965 МДж/моль. Потенциалы ионизации атомов в единицах кДж/моль имеются в справочнике (Эмсли, 1993).
Таблица 1.11
Расчетные и экспериментальные данные о работе
выхода электрона j(эВ) для некоторых кристаллов
| Кристалл(формула) |
W, МДж/моль,расчет по (1.10) |
n,число валентных электронов |
Работа выхода электронаj, эВ |
Кристалл(формула) |
W, МДж/моль,расчет по (1.10) |
n,число валентных электронов |
Работа выхода электронаj, эВ |
| Расчет по (1.15) |
Эксперимент |
Расчет по (1.15) |
Эксперимент |
| SiO2 |
46,73 |
12 |
5,0 |
5,0 |
CdS |
29,72 |
8 |
4,8 |
4,1 |
| MgO |
21,28 |
6 |
4,6 |
4,4 |
Ag2S |
17,61 |
10 |
2,3 |
3,8 |
| BeO |
21,32 |
6 |
4,6 |
4,7 |
MoS2 |
33,36 |
14 |
4,2 |
4,5 |
| Al2O3 |
65,92 |
18 |
4,7 |
4,7 |
ZnTe |
24,56 |
8 |
4,0 |
3,6 |
| TiO2 |
45,7 |
12 |
4,9 |
3,9-6,2 |
a-Fe |
10,9 |
4 |
3,5 |
4,1 |
| CaO |
20,21 |
6 |
4,3 |
3,4 |
CuО |
20,92 |
6 |
4,5 |
4,35 |
| CdO |
20,61 |
6 |
4,4 |
4,0 |
Nb |
14,43 |
5 |
3,7 |
4,2 |
| FeO |
20,72 |
6 |
4,4 |
3,9 |
B2O3 |
66,2 |
18 |
4,4 |
4,7 |
| WO2 |
50,17 |
12 |
5,4 |
5,0 |
Ta2O5 |
98,2 |
30 |
4,2 |
4,65 |
| Cu2O |
25,27 |
6 |
5,4 |
5,0 |
TiN |
30,44 |
9 |
4,4 |
4,1 |
| La2O3 |
48,981 |
18 |
3,5 |
3,1 |
К |
1,43 |
1 |
1,8 |
2,2 |
| Mg2SiO4 |
87,43 |
24 |
4,7 |
- |
ZnO |
20,84 |
6 |
4,5 |
4,1 |
| BN (гекс.) |
33,8 |
8 |
5,5 |
6,4 |
SiC |
25,64 |
8 |
4,5 |
4,0 |
| AlN |
31,5 |
8 |
5,1 |
5,35 |
a-Fe2O3 |
65,4 |
18 |
4,7 |
4,5 |
| Na2S |
13,22 |
6 |
2,8 |
3,0 |
NaJ |
9,868 |
6 |
2,1 |
1,5 |
| PbS |
20,84 |
8 |
3,4 |
3,5 |
MgAl2O4 |
86,45 |
24 |
4,7 |
- |
| ZnS |
29,85 |
8 |
4,8 |
≈4 |
BeAl2O4 |
87,0 |
24 |
4,7 |
- |
Итак, имеется принципиальная возможность, используя соответствующие данные в формуле (1.16), проверять достоверность параметров
W, вычисляемых по формуле (1.10). С другой стороны, можно также решать проблему независимой оценки энергии атомизации кристаллов с помощью формулы (1.16), соответствующие оценки приведены в таблице 1.12, где наблюдается вполне удовлетворительная сходимость расчетных и экспериментальных величин
Еа. Однако эти результаты не следует абсолютизировать и рекомендовать этот метод в качестве надежного для нахождения энергий атомизации кристаллов из энергий сцепления остовов и электридов. Дело в том, что точность оценок
W по формуле (1.10) составляет, по нашим данным, величину порядка 1-5%. Но по данным таблицы 1.12 такую же приблизительно величину составляет доля энергии атомизации в энергии сцепления остовов и электридов, поскольку
W>>
E. Отсюда неизбежны большие погрешности при оценке энергии атомизации по формуле (1.16) при использовании соответствующих величин
W.
Поскольку мольные величины
W у различных простых и сложных кристаллических соединений в принципе не сопоставимы, необходимо пользоваться удельными энергиями сцепления остовов и электридов, отнесенными к единичной массе (1 г) или единичному объему (1 см
3) вещества минерала. Переход от
W (МДж/моль) к удельной мас-
Таблица 1.12
Расчетные и экспериментальные данные по
энергии атомизации некоторых кристаллов
| Кристалл (формула) |
Локализованные в узлах решетки атомные остовы кристалла |
W, МДж/моль, расчет по формуле (1.10) |
ΣIn, МДж/моль (Свойства элементов, 1976) |
Энергия атомизации Еа, МДж/моль |
| Расчет по формуле (1.16) |
Экспери-мент |
|
SiO2
|
[Si4+][O4+]2
|
46,73 |
44,9 |
1,83 |
1,88 |
|
MgO
|
[Mg2+][O4+]
|
20,82 |
19,66 |
1,16 |
1,0 |
|
BeO
|
[Be2+][O4+]
|
21,32 |
20,13 |
1,19 |
1,18 |
|
Al2O3
|
[Al3+]2[O4+]3
|
65,92 |
62,7 |
3,22 |
3,22 |
|
TiO2
|
[Ti4+][O4+]2
|
45,70 |
43,81 |
1,89 |
1,91 |
|
CaO
|
[Ca2+][O4+]
|
20,21 |
19,21 |
1,0 |
1,06 |
|
CdO
|
[Cd2+][O4+]
|
20,61 |
19,97 |
0,64 |
0,62 |
|
FeO
|
[Fe2+][O4+]
|
20,72 |
19,8 |
0,92 |
0,94 |
|
Cu2O
|
[Cu1+]2[O4+]
|
25,27 |
24,07 |
1,2 |
1,1 |
|
La2O3
|
[La3+]2[O4+]3
|
61,8 |
59,33 |
2,47 |
3,4 |
|
Mg2SiO4
|
[Mg2+]2[Si4+][O4+]4
|
87,43 |
82,36 |
4,51 |
3,93 |
|
BN
|
[B3+][N5+]
|
33,8 |
32,64 |
1,16 |
1,29 |
|
AlN
|
[Al3+][N5+]
|
31,5 |
30,89 |
0,6 |
1,1 |
|
PbS*
|
[Pb(2+2)+][S4+]
|
20,84 |
20,19 |
0,65 |
0,57 |
|
ZnS
|
[Zn2+][S6+]
|
29,85 |
29,32 |
0,53 |
0,61 |
|
FeS2*
|
[Fe(2+2)+][S5+]2
|
47,99 |
46,86 |
1,13 |
1,13 |
|
MoS2
|
[Mo4+][S4+]2
|
33,36 |
31,9 |
1,46 |
1,48 |
|
ZnTe
|
[Zn2+][Te6+]
|
29,73 |
29,33 |
0,40 |
0,47 |
|
a-Fe
|
[Fe4+]
|
10,9 |
10,68 |
0,22 |
0,42 |
|
C (алмаз)
|
[C4+]
|
15,01 |
14,28 |
0,73 |
0,72 |
|
Fe2O3
|
[Fe3+]2[O4+]3
|
65,4 |
62,98 |
2,42 |
2,41 |
|
MgAl2O3
|
[Mg2+][Al3+]2[O4+]4
|
86,56 |
82,36 |
4,2 |
4,09 |
|
ZrSiO4
|
[Zr4+][Si4+][O4+]4
|
91,52 |
87,17 |
4,35 |
4,11 |
|
WC*
|
[W(4+2)+][C4+]
|
34,61 |
32,95 |
1,66 |
1,61 |
|
Fe3C*
|
[Fe(2+2)+]3[C4+]
|
47,95 |
45,98 |
1,97 |
1,94 |
|
CaF2
|
[Ca2+][F3+]2
|
25,91 |
23,95 |
1,96 |
1,56 |
|
MgF2
|
[Mg2+][F3+]2
|
25,84 |
24,4 |
1,44 |
1,43 |
|
SnO2
|
[Sn4+][O4+]2
|
45,88 |
43,94 |
1,94 |
1,38 |
|
NaCl
|
[Na1+][Cl5+]
|
20,2 |
19,56 |
0,64 |
0,64 |
|
Al2SiO4F2
|
[Al3+]2[Si4+][O4+]4[F3+]2
|
117,71 |
112,35 |
5,36 |
5,36 |
* -
в этих кристаллах общий заряд атомного остова катиона (в круглых скобках) дан в виде суммы, где первое слагаемое отвечает валентности металла по отношению к неметаллу, а второе слагаемое - металлической валентности (взаимодействию М-М)
совой энергии сцепления остовов и электридов
Wm и удельной объемной энергии сцепления остовов и электридов
Wv осуществляется посредством следующих формул:
Wm = W/M, МДж/г; (1.17)
Wv = W/V, МДж/см3, (1.18)
где:
M - формульная (мольная) масса соединения, г/моль, а
V - его мольный объем, см3/моль, определяемый по формуле
V =
M/ρ (здесь ρ - плотность вещества, г/см3).
Отсюда следуют указанные размерности
Wm и
Wv и соотношение между ними:
Wv = Wmρ (1.19)
Как следует из предыдущих работ (Зуев, Мочалов, Щербатов, 1998; Зуев, Аксенова, Мочалов и др., 1999) для количественной оценки физических свойств кристаллов путем построения соответствующих корреляционных зависимостей необходимо использовать именно удельные энергии сцепления остовов и электридов. В таблице 1.13 приводятся результаты расчетов этих энергий для наиболее распространенных рудных и нерудных минералов.
Таблица 1.13
Удельные энергии сцепления остовов и электридов для некоторых
наиболее распространенных рудных и нерудных минералов
| Рудные минералы |
Нерудные минералы |
| Минерал, формула |
Wm,МДж/г |
Wv,МДж/см3 |
Минерал, формула |
Wm,МДж/г |
Wv,МДж/см3 |
|
Галенит PbS
|
0,09 |
0,66 |
Кварц SiO2
|
0,78 |
2,06 |
|
Сфалерит ZnS
|
0,31 |
1,23 |
Кальцит CaCO3
|
0,68 |
1,85 |
|
Халькопирит CuFeS2
|
0,24 |
1,05 |
Микроклин KAlSi3O8
|
0,67 |
1,71 |
|
Борнит Cu5FeS4
|
0,18 |
0,91 |
Альбит NaAlSi3O8
|
0,69 |
1,81 |
|
Халькозин Cu2S
|
0,13 |
0,76 |
Анортит CaAl2Si2O8
|
0,65 |
1,79 |
|
Пирит FeS2
|
0,39 |
1,95 |
Форстерит Mg2SiO4
|
0,62 |
2,0 |
|
Арсенопирит FeAsS
|
0,29 |
1,82 |
Доломит CaMg(CO3)2
|
0,75 |
2,14 |
|
Троилит FeS
|
0,25 |
1,2 |
Энстатит MgSiO3
|
0,67 |
2,16 |
|
Пентландит (Fe,Ni)9S8
|
0,23 |
1,16 |
Диопсид CaMgSi2O6
|
0,62 |
2,04 |
|
Железо Fe
|
0,2 |
1,57 |
Эпидот Ca2Al2FeSi3O12(OH)
|
0,6 |
2,17 |
|
Медь Cu
|
0,13 |
1,16 |
Ангидрит CaSO4
|
0,5 |
1,5 |
|
Платина Pt
|
0,06 |
1,29 |
Тремолит Ca2Mg5Si8O22(OH)2
|
0,66 |
1,98 |
|
Сперрилит PtAs2
|
0,15 |
1,63 |
Антофиллит Mg7Si8O22(OH)2
|
0,69 |
2,03 |
|
Тетраэдрит Cu12Sb3S13
|
0,22 |
1,09 |
Мусковит KAl3Si3O10(OH)2
|
0,68 |
1,92 |
|
Скуттерудит Co4[As4]3
|
0,24 |
1,65 |
Флогопит KMg3AlSi3O10(OH)2
|
0,64 |
1,78 |
|
Аргентит Ag2S
|
0,08 |
0,56 |
Биотит KFe3AlSi3O10(OH)2
|
0,52 |
1,72 |
|
Прустит Ag3AsS3
|
0,13 |
0,75 |
Серпентин Mg6Si4O10(OH)8
|
0,78 |
2,03 |
|
Аурипигмент As2S3
|
0,09 |
0,32 |
Каолинит Al4Si4O10(OH)8
|
0,78 |
2,03 |
|
Молибденит MoS2
|
0,26 |
1,3 |
Гроссуляр Ca3Al2Si3O12
|
0,61 |
2,18 |
|
Ковеллин CuS
|
0,19 |
0,88 |
Волластонит CaSiO3
|
0,58 |
1,68 |
|
Миллерит NiS
|
0,2 |
1,08 |
Нефелин NaAlSiO4
|
0,6 |
1,58 |
|
Никелин NiAs
|
0,21 |
1,68 |
Кианит Al2SiO5
|
0,66 |
2,43 |
[1] Атомный остов получается удалением из нейтрального атома внешних (валентных) электронов. Другими словами, атомный остов - это «ядро + внутренние, не участвующие в химической связи электроны».
[2] Фактически речь идет о наглядном кристаллохимическом моделировании представлений единой зонной теории твердых тел.
[3] Во избежание излишнего загромождения раздела формула дается в постулированном виде с необходимыми заменяющими ее подробный вывод комментариями.
[4] Согласно В. С. Урусову
Ne
o2/Å = 332,06 ккал/моль = 1,389 МДж/моль.
[5] Для гомоатомных ковалентных и металлических кристаллов
fi = 0 и
р* = 1. Граничные условия параметра
fi в формуле (1-
fi2)
0.5 - 0 ≤
fi < 1.





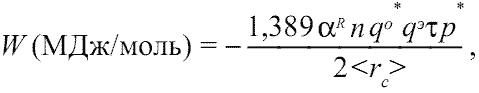 (1.9)
(1.9)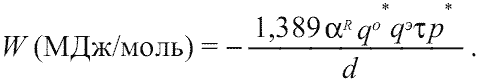 (1.10)
(1.10)