3.5. Структура, энергетические параметры и свойства магнезиального вяжущего вещества
По составу и химической природе магнезиальные вяжущие 3MgO∙MgCl
2∙11H
2O и 5MgO∙MgCl
2∙13H
2O следует относить к гидратированным гидроксохлоридам магния (Уэллс, 1987). Имеется расшифровка структуры наиболее стабильного (как это принято считать) соединения 3MgO∙MgCl
2∙11H
2O (Wolff et al, 1953), она низкосимметричная, триклинной сингонии с параметрами: a
o = 8,65 Å, b
o = 6,27 Å, c
o = 7,43 Å, α =101
о58', β = 104
о, γ = 73
о11', Z = 2
[1], рассчитанная плотность ρ = 1,86 г/см
3.
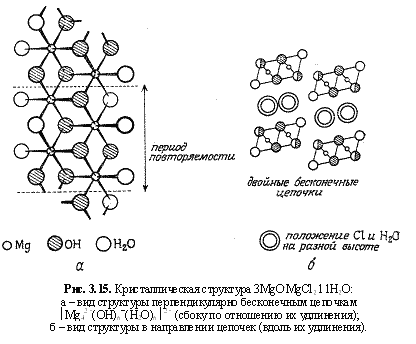
Согласно этой работе, основу структуры рассматриваемой фазы (и, по-видимому, ряда других гидратированных гидроксосолей магния) составляют двойные цепи состава Mg
4(OH)
3(H
2O)
3, которые соединяются между собой ионами Cl
- и молекулами воды (рис. 3.15). Используя условные обозначения структурного мотива соединения по Д.П.Григорьеву (Григорьев, 1966), структурную кристаллохимическую формулу рассматриваемого соединения следует записать в виде
|Mg42+(OH)6-(H2O)6|2+Cl21-×2H2O,
где катионый радикал из бесконечных сдвоенных магниево-гидроксидных цепочек выделен прямыми скобками.
Из представленной структурной формулы следует, что основу сцепления цепочек составляет их электростатическое взаимодействие с ионами хлора и вандерваальсовское (молекулярное) с молекулами воды. Этим объясняется волокнистое строение и сравнительно низкая твердость магнезиального цемента - Н
М = 2,5-3 по относительной минералогической шкале Мооса и HV = 45-78 кгс/мм
2 (абсолютная твердость или микротвердость вдавливания алмазной пирамиды по Виккерсу).
[2]
Ввиду отсутствия соответствующих структурных данных, для второй, менее стабильной модификации магнезиального цемента 5MgO×MgCl
2×13H
2O можно предложить (при условии сохранения цепной структуры) следующую структурную формулу:
|Mg62+(OH)10-(H2O)6|2+Cl21-×2H2O,
где в прямых скобках выделен бесконечный радикал из сдвоенных магниево-гидроксидных цепочек, скрепленных анионами Сl
- и молекулами воды.
Из сравнения обеих структурных формул следует: полная идентичность структурных мотивов соединений, равенство зарядов катионных цепочечных радикалов и скрепляющих их анионов хлора, а также числа межцепочечных молекул воды. Следовательно, свойства сравниваемых соединений, вытекающие из тесной близости их конституции, должны быть практически одинаковыми или, по крайней мере, весьма близкими.
Следует особо подчеркнуть, что обусловленная цепочечной кристаллической структурой магнезиальных цементов их характерная спутано-волокнистая текстура четко наблюдается лишь в электронном микроскопе при очень больших увеличениях (Маткович, Рогич, 1974). Впрочем, признаки такой текстуры наблюдались нами и в обычном оптическом микроскопе, что отражено на микрофотографии (рис. 3.9).
В таблице 3.4 приведены основные энергетические параметры и вычисленные с их помощью по формулам из 2-ой главы некоторые физические свойства для фазы 3MgO∙MgCl
2∙11H
2O и (для сравнения) - соответствующие данные для одной из основных фаз портландцемента, имеющую, согласно (Белов, 1976; Теория цемента, 1991), состав 12CaO∙6SiO
2∙7H
2O, а в таблице 3.5 даны сравнительные показатели магнезиальных цементов и некоторых природных материалов.
В порядке обсуждения данных таблицы 3.4 необходимо привести соответствующие комментарии и дать следующие пояснения и оговорки.
Таблица 3.4
Сравнительная харктеристика состава и свойств магнезиального и кальциево-силикатного цементов
| Энергетические и физические характеристики |
Цемент |
| Магнезиальний |
Кальциево-силикатный |
| Валовой состав |
3MgO·MgCl2·11H2O |
12CaO·6SiO2·7H2O |
| Структурная формула |
[Mg42+(OH)6ˉ(H2O)6]2+Cl2ˉ·2H2O |
Ca[Si6O17](OH)14
(гиллебрандит) |
| Удельные энергии атомизации: |
| Ev, кДж/см3 |
67,46 |
69,10 |
| Em, кДж/г |
36,27 |
25,69 |
| Удельные энергии сцепления остовов и электридов: |
| Wv, МДж/см3 |
1,51 |
1,55 |
| Wm, МДж/г |
0,81 |
0,58 |
| Удельные энергии кристаллической решетки: |
| Uv, кДж/см3 |
- |
259,00 |
| Um, кДж/г |
- |
96,22 |
| Структурная рыхлость ω, см3/г-ат |
11,13 |
8,8 |
| Кристаллическая струтура |
Резко анизодесмическая, образована сдвоенными цепочками октаэдров Mg(OH, H2O)6, соединенных ионами хлора и молекулами воды |
Квазикоординационная, слабо анизодесмическая, ленточная, представлена чередованием ксонотлитовых и портландитовых элементов: Ca[Si6O17](OH)2·6Ca(OH)2 |
| Ионность связи fi |
0,98 |
0,80 |
| Макроструктура |
Спутано-волокнистая |
Массивная |
| Плотность ρ, г/м3 |
1,86 |
2,69 |
| Относительная твердость по минералогической шкале |
2-3 |
5 |
| Микротвердость по Викерсу HV, кг/мм2 |
40-50(0,45 ГПа) |
300-500(3,5 ГПа) |
| Трещиностойкость К1с, МПа·м1/2 |
0,88 |
0,92 |
| Хрупкость HV (ГПа)/ K1с |
0,5 |
3,8 |
| Теплопроводность λ, Вт/(м·К) |
0,5-1,6 |
1,3-1,8 |
| Температура разложения или плавления, ºС |
500 (Тразл.) |
1270(Тпл.) |
| Температурный коэффициент объемного расширения, αv, 10-6·К-1 |
30 |
30 |
| Модуль растяжения Е, ГПа |
140 |
150 |
| Модуль сжатия G, ГПа |
45 |
60 |
| Модуль всестороннего объемного сжатия К, ГПа |
105 |
115 |
| Предел прочности на разрыв σр, МПа |
6,5 |
11,3 |
| Предел прочности при сжатии, σсж, МПа |
25-35 |
85-90 |
| Коэффициент Пуассона σп |
0,29 |
0,29 |
| Объемная сжимаемость β, 10-12·Па-1 |
7 |
6,5 |
| Поверхностная энергия Eshkl, Дж/м2 |
1,1 |
1,2 |
| Скорость звука v, км/с |
5,5-6 |
6-6,5 |
| Максимальная частота колебаний атомов vm, Гц |
17-18 |
14 |
| Грамм-атомная теплоемкость Ср, Дж/(г-ат)К |
18-22 |
17-20 |
| Работа выхода электрона φ, эВ |
4,5 |
4,5 |
ПРИМЕЧАНИЕ. Ввиду идентичности структур и близости энергетических характеристик магнезиальных цементов 3MgO·MgCl2·11H2O и 5MgO·MgCl2·13H2O их физические свойства, по всей вероятности, также близки.
За исключением твердости магнезиальных цементов (см. текст), характеризующие различные физические свойства параметры сравниваемых цементов рассчитывались по соответствующим формулам главы 2 с усреднением величин, получаемых с использованием различных энергетических параметров, как это продемонстрировано на примере периклаза MgO в таблице 2.8. Другие вероятные фазы Са-силикатных цементов (впрочем, близкие по составу к гиллебрандиту) указаны в книге (Теория цемента, 1991).
Таблица 3.5
Сравнительные показатели магнезиальных цементов и природных материалов
| Наименование показателей |
Магнезиальные цементы «Альфа Пол» |
Природные материалы
(Берлин, Сычев, 1986) |
| Физико-механические характеристики |
| Прочность на сжатие, МПа |
40-60 |
Гранит > 100 |
| (марка) |
(В 30) |
Мрамор 60-100 |
|
|
Доломит 40-80 |
| Прочность на изгиб, МПа |
10-15 |
- |
| Строительные свойства |
| Истираемость Rист. |
0,4-0,7 |
Гранит 0,2-0,4 |
|
|
Мрамор 1,0-3,0 |
|
|
Регламентируемое значение 0,5 |
| Морозостойкость, марка |
«Альфа-Пол К» F 300 |
>> F 300 |
|
«Альфа-Пол М» F 200 |
|
| Водостойкость, Кв |
«Альфа-Пол К» 0,68 |
Гранит 0,8-0,9 |
|
«Альфа-Пол М» 0,8 |
Мрамор 0,8-0,9 |
|
|
Доломит 0,7-0,9 |
| Водопоглощение, % |
«Альфа-Пол К» 5 |
Гранит 0,1-0,6 |
|
«Альфа-Пол М» 5 |
Мрамор 0,1-0,3 |
|
|
Доломит 1,0-9,0 |
|
|
Бетон тяжелый 2,0-3,0 |
| Средняя плотность (с |
1,9-2,2 |
Гранит 2,7 |
| порами и пустотами), ρ г/см3 |
|
Мрамор 2,7 |
|
|
Доломит 2,1-2,7 |
Как следует из предыдущей 2-ой главы, корректная оценка твердости (как относительной, так и абсолютной) кристаллических фаз по энергетическим параметрам, строго говоря, возможна лишь для изодесмических координационных кристаллов и не возможна для анизодесмических (островных, цепочечных и слоистых) кристаллических веществ. Это связано с тем, что при механическом разрушении последних нарушаются, согласно известному кристаллохимическому правилу, слабые связи между соответствующими группировками молекулярного характера и не затрагиваются прочные связи внутри островных, цепочечных и слоистых атомных группировок. А используемые в расчетах твердости энергетические параметры (энергоплотность и др.) учитывают все (слабые межмолекулярные и прочные внутримолекулярные) связи анизодесмического соединения.
Поэтому в случае магнезиального цемента в таблице 3.4 приведены не расчетные, а полученные экспериментально величины твердости, которые, очевидно, соответствуют «раздвиганию» цепочек и нарушению ионных и молекулярных связей между цепочками. При этом прочные ионно-ковалентные связи внутри цепочек сохраняются.
Здесь необходимо оговориться, что подход с использованием электроотрицательностей (см. раздел 2.6) позволяет рассчитать твердость (а также термическую стабильность) анизодесмических кристаллических соединений, что будет продемонстрировано на двух примерах цепочечного магнезиального вяжущего и островного бишофита.
Представим цепочечный кристалл |Mg
42+(OH)
6-(H
2O)
6|
2+Cl
21-·как соединение валентного типа AХ
2, в котором A - цепочечный радикал, Х - ионы хлора (связями между цепочками за счет молекул воды можно пренебречь в силу незначительного их вклада в твердость соединения).
Среднегеометрическая электроотрицательность цепочечного радикала с использованием величин кристаллических ЭО составляющих атомов (Бацанов, 1986, с. 140): <ЭО>(А) = (0,8
4x3,6
12x2,1
18)
(1/34) = 2,27, <ЭО>(Х) = 2,6. Тогда <ЭО>(АХ
2) = (2,27x2,6
2)
(1/3) = 2,5 и по формулам (2.123) и (2.124) имеем:
Н
М = 0,75x2,5
3(1 - 0,98
2)
1/2 = 2,3
Т
разл. = 563x2,52(1 - 0,98
2)
1/2 = 700
оК (427
оС)
Вычисленные параметры относительной твердости и температуры разложения магнезиального вяжущего находятся в удовлетворительном согласии с соответствующими экспериментальными данными. Принятый в расчетах параметр ионности (f
i = 0,98) подтверждает почти 100%-ный ионный характер связей цепочечного радикала и ионов хлора.
Аналогичным образом рассчитаем твердость и температуру разложения бишофита - второго после каустического магнезита важнейшего компонента для производства магнезиального вяжущего. Его истинную (структурную) формулу следует записывать как [Mg(H
2O)
6]
2+Cl
21-, где в квадратных скобках заключены островные октаэдрические аква-комплексы магния. Следовательно, бишофит является островным ионным соединением валентного типа АХ
2, в котором А - [Mg(H
2O)
6]
2+, X - Cl
1-. Среднегеометрическая электоотрицательность островного комплекса <ЭО>(А) = (0,8x2,1
12x3,6
6)
1/19 =2,37, <ЭО>(Х) = 2,6, <ЭО>(АХ
2) = (2,37x2,6
2)
1/3 = 2,52. Приняв f
i = 0,99, получаем для бишофита:
НМ = 0,75x2,523(1 - 0,992)1/2 = 1,7
Тразл. = 563x2,522(1 - 0,992)1/2 = 504оК (231оС)
Обе расчетные величины близки к соответствующим справочным данным (Поваренных, 1966; Свойства неорганических соединений, 1983).
Как и следовало ожидать, портландцемент (в виде гиллебрандита Ca1
2Si
6O
17(OH)
14) характеризуется заметно меньшей средней ионностью (f
i = 0,8). Расчеты среднегеометрической электроотрицательности этого квазикоординационного соединения, его относительной твердости и температуры плавления дают:
<ЭО> = (0,712x1,76x3,631x2,114)(1/63) = 2,18,
НМ = 0,75x2,183(1 - 0,82)1/2 = 4,7,
Тразл. = 563x2,182(1 - 0,82)1/2 = 1605оК (1332оС)
Найденные таким путем величины относительной твердости и температуры плавления гиллебрандита близки к рассчитанные по другим энергетическим параметрам (таблица 3.4).
В заключение проведем сравнительный анализ магнезиального и кальциево-силикатного цементов по рассчитанным для них в таблице параметрам - энергетическим характеристикам и свойствам.
- По одной группе параметров (Ev, Wv, αv, E, G, K, σп, b, Eshkl, v, Cp, φ), более или менее близких у обоих цементов, они не имеют значимых преимуществ друг перед другом.
- По другой группе параметров (ω, HM, HV, Тпл., σр, σсж) портландцемент предпочтительнее.
- По третьей группе параметров (Em, Wm, ρ, νm, λ, хрупкости) предпочтительнее магнезиальный цемент. Кроме того, он гораздо лучше полируется, что имеет немаловажное значение при его практическом использовании.
Из приведенных данных можно лишь констатировать, что по одним параметрам определенными преимуществами обладает портландцемент, по другим - магнезиальный цемент. Но сама постановка вопроса о том, что какой-то один цемент лучше другого в принципе не правомерна, так как многие их свойства и соответственно области применения различны. Именно поэтому, учитывая сказанное, необходимо детально изучать их энергетические характеристики и физико-химические свойства для корректного использования того или иного цемента в тех или иных конкретных ситуациях.
В частности, особо следует подчеркнуть явное преимущество магнезиального цемента (по сравнению с портландцементом) по удельным массовым энергетическим параметрам E
m и W
m, что сближает его с весьма стабильными минералами (Зуев, Денисов, Мочалов и др., 2000), которые являются наиболее устойчивыми природными химическими соединениями в составе земной коры, а также верхней мантии.
Как следствие, магнезиальный цемент характеризуется высокими параметрами максимальной частоты колебания атомов (таблица 3.6), что, по-видимому, является ключом к объяснению повышенных защитных (экранирующих) свойств материалов на основе магнезиального цемента в смеси с шунгитом от вредного воздействия электромагнитных излучений радиочастотного диапазона.
Таблица 3.6
Энергетические и частотные характеристики графита, шунгита, магнезиального цемента и портландита
| Вещество |
Ea, кДж/моль |
Em, кДж/г |
ρ, г/см3 |
Ev, кДж/см3 |
vm, ТГц |
| Графит |
718,6 |
59,8 |
2,27 |
136 |
23,2 |
| Шунгит |
700 |
58,3 |
1,95 |
114 |
23,7 |
| Магнезиальный цемент |
15021 |
36,3 |
1,86 |
67,5 |
17,6 |
| Гиллебрандит |
29791 |
25,7 |
2,69 |
69 |
14 |
ПРИМЕЧАНИЕ. Для графита приведены данные согласно (Мамыров, 1991), для остальных соединений - рассчитанные нами параметры.
Из данных таблицы 3.6 однозначно следует вывод, что по параметрам удельной массовой энергии атомизации (E
m) и частотным характеристикам (ν
m) магнезиальный цемент превосходит традиционный цемент типа портландита.
Как показали исследования нашей фирмы, изготовленные с применением магнезиального цемента с шунгитовым наполнителем защитные (изолирующие) панели (экраны) способны обеспечивать многократное ослабление вредных для человека воздействий электромагнитных и высокочастотных полей.
Возможное объяснение этому эффекту следует искать, как уже указывалось, в высоких параметрах E
m и ν
m шунгита и магнезиального цемента.
Если принять состав защитных экранов состоящими наполовину из магнезиального цемента и наполовину из шунгита, то средние параметры такого материала будут: E
m = 47 кДж/г, ν
m = 21 ТГц. Согласно данным (Мамыров, 1991), наиболее высокие параметры ν
m характерны для самых высокоэнергоплотных неорганических веществ (минералов) - алмаза (ν
m = 26,9 ТГц) и графита (ν
m = 23,16 ТГц). Как следует из таблицы 3.6, энергетические и частотные характеристики шунгита и графита близки. Но графит обладает резко анизодесмической слоистой структурой и очень слабыми межслоевыми молекулярными связями, что делает его «прозрачным» для излучений по межслоевым направлениям. Однако подвергнутый специальной технологической обработке (прессованию и др.) графит уже давно и успешно используется как замедлитель нейтронного излучения в ядерных реакторах, как эффективное огнеупорное вещество и т.д.
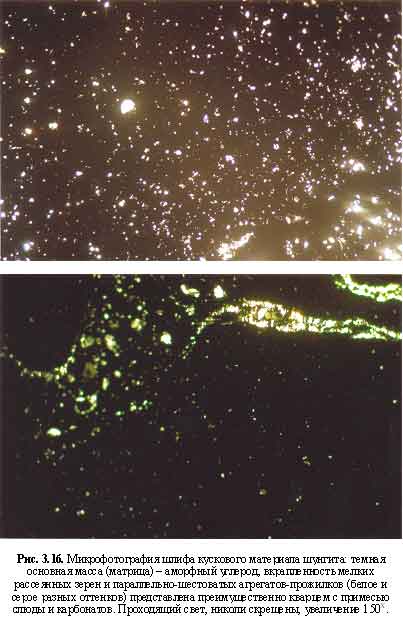
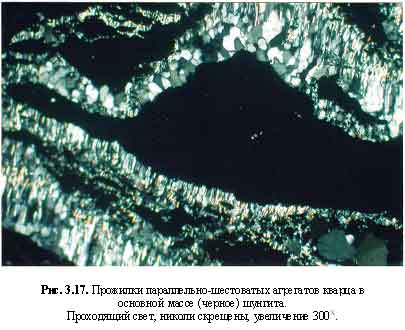
В отличие от графита шунгит является изотропным аморфным стекловатым веществом (Шумилова, 2003). Рис. 3.16-3.17 демонстрируют серию микрофотографий кускового материала шунгита, содержащего в качестве наиболее обычной примеси тонко вкрапленный кварц, а также его прожилковые формы выделений. Приведенные микрофотографии шунгита не отражают истинного содержания в нем кварца, на самом деле он присутствует в шунгите в незначительном количестве.
Шунгит, как весьма специфическая природная форма углерода, представляет собой хаотическую, беспорядочную сетку гибридных ковалентных sp
x-связей атомов углерода. Поэтому шунгит является гораздо более совершенным материалом для выполнения защитных (экранирующих от различного рода излучений) функций. Объяснение последних, как следует из приведенных аргументов, дано в самом общем виде и в дальнейшем будет детализировано.
Обращает на себя внимание (таблица 3.6) близость (совместимость) не только частотных характеристик, но также плотностей шунгита и магнезиального цемента, что по-видимому является благоприятным фактором при изготовлении защитных материалов из смесей этих веществ.
[1] В указанной оригинальной работе принята рентгеновская формула соединения Mg
2(OH)
3Cl∙4H
2O, для стехиометрии 3MgO∙MgCl
2∙11H
2O Z = 1.
[2] Согласно кристаллохимической теории твердости (Поваренных, 1963; Урусов, 1975), наиболее твердые кристаллические соединения обладают ковалентными связями, а менее твердыми являются соединения с ионными, металлическими и молекулярными связями.



